Publication H4
En quoi les études de marché qualitatives dérisquent l’innovation en santé ?
Par Maxime Ros – H4 | La Source (Lausanne)
Résumé
Dans l’écosystème santé, réduire le risque d’un nouveau produit ou service ne se résume pas à vérifier un « fit » technologique, autrement dit l’adéquation entre les besoins et une solution. Il s’agit de valider tôt, et en profondeur, les usages réels, les contraintes cliniques, réglementaires et économiques, puis d’itérer jusqu’à ce que la solution réponde précisément aux attentes des parties prenantes (patients, soignants, payeurs, autorités, acheteurs).
Les études de marché qualitatives (entretiens, observations contextuelles, tests d’usage, focus groups, co-conception‑) sont le levier le plus direct pour y parvenir : elles révèlent les motivations, les objections, les attentes, les besoins, les requis, les freins, la réalité des parcours de soin, dans leurs étapes et leur vécu, les freins tout comme les critères d’adoption. Elles montrent la complexité bien au-delà des chiffres d’un questionnaire quantitatif. —. La littérature scientifique et les meilleures pratiques d’innovation clinique confirment cette valeur : la recherche qualitative comble les angles morts des approches quantitatives, elle nourrit les décisions centrées utilisateurs, et favorise l’adoption en conditions réelles. [academic.oup.com]. C’est tout cet ensemble qui contribue à la définition de ce qui s’appelle le mix marketing : une combinaison de 4 éléments propres à la solution innovante (le Produit, son Prix, sa Place sur le marché, sa valorisation au travers de sa Promotion).
H4 n’est pas un programme d’incubation/accélération : nous sommes un hub offrant des études qualitatives lorsque start-ups et Business Unit doivent documenter la preuve d’usage, la désirabilité, l’acceptabilité clinique et la faisabilité d’adoption—notamment via des outils issus du Design Thinking / Human Centered Design.
1) Pourquoi « qualifier l’usage » dérisque tout autant que « quantifier la demande »
Dans la santé, les échecs d’adoption ne proviennent pas seulement du manque d’efficacité clinique : incompréhension des routines de soins, interfaces inadaptées, flux de travail perturbés, contraintes de remboursement mal anticipées, faible confiance des utilisateurs… Autant de facteurs que la donnée qualitative est la mieux placée pour révéler, expliquer et traiter. Les revues récentes insistent : la recherche qualitative explore le « pourquoi » et le « comment » derrière les chiffres (expériences vécues, normes de service, arbitrages), éclairant les décisions cliniques et organisationnelles qui déterminent la réussite au‑delà des trials. [thelancet.com]
Côté innovation digitale et medtech, les barrières d’adoption—interopérabilité, littératie numérique (capacité d’une personne à comprendre, utiliser et interagir efficacement avec les technologies numériques), confiance, ergonomie, workflows—sont désormais bien documentées ; s’y attaquer implique co-concevoir avec les utilisateurs finaux (soignants, patients partenaires, responsables administratifs et opérationnels…) et évaluer en continu les usages réels plutôt que d’ajouter des fonctionnalités. [ejbi.org], [academic.oup.com]
Implication pour un startuper ou un chef produit : avant d’élargir l’échantillon d’une enquête en ligne, validez la valeur d’usage dans le contexte réel (service, salle d’op, domicile, pharmacie hospitalière, etc.). C’est le meilleur « gain de temps » contre les cycles produits trop longs.

Source : https://technologyadvice.com/blog/information-technology/qualitative-vs-quantitative/
2) Démystifier le ‘mix marketing des 4 P’ plus complexe qu’ailleurs
Le marketing mix en santé que nous définissons ici par la combinaison des 4 P : Produit, Prix, Place, Promotion, comporte des contraintes spécifiques qui expliquent pourquoi l’« écoute fine » (qualitative) est indispensable. Le marketing mix en santé que nous définissons ici par la combinaison des 4 P : Produit, Prix, Place, Promotion, comporte des contraintes spécifiques qui expliquent pourquoi l’« écoute fine » (qualitative) est indispensable.
P – Produit (preuve clinique + utilisabilité + conformité)
- Usability / facteurs humains : les normes IEC 62366‑1 exigent un processus de conception centrée utilisateur visant à réduire les erreurs d’usage et à prouver l’aptitude à l’emploi—enjeu de sécurité et de mise sur le marché. Les tests utilisateurs (tâches critiques) et la validation d’usage sont des livrables réglementaires. [iso.org], [greenlight.guru]
- Design Thinking & Human Centered Design : en santé, les approches centrées humain améliorent la pertinence et l’équité d’accès, via l’observation in situ, l’idéation itérative et les prototypes testés avec les parties prenantes.
P – Prix (market access & remboursement)
- Les lancements pharma/medtech échouent souvent faute d’une stratégie market access qui anticipe les preuves cliniques/économiques attendues par payeurs et autorités (HTA), ainsi que les parcours de distribution. Le pricing dépend de cette équation, à co‑construire avec les acteurs très en amont. [deloitte.com]
P – Positionnement (Place – canaux, achats, intégration dans les flux)
- En B2B santé, le positionnement recouvre l’intégration dans les SI, les processus d’achats hospitaliers, les protocoles, l’interopérabilité—tout ce que les études qualitatives défrichent en analysant qui fait quoi, où, quand, avec quoi. Les barrières techniques et organisationnelles sont critiques pour l’adoption.
P – Promotion (KOLs, evidence storytelling, éducation)
- L’influence des Key Opinion Leaders, la formation et l’évidence narrative adaptée aux différents publics (cliniciens, biomédical, direction, payeurs, patients) sont déterminantes ; les contenus et canaux doivent être prototypés avec les cibles pour éviter le décalage message – usage. [mckinsey.org]
Conclusion : en santé, le mix marketing tel que défini ici, est une ingénierie d’alignement entre Produit, Prix, Positionnement, Promotion. Sans compréhension qualitative des acteurs et contextes, on sous‑estime les frictions et on sur‑promet sur les bénéfices.
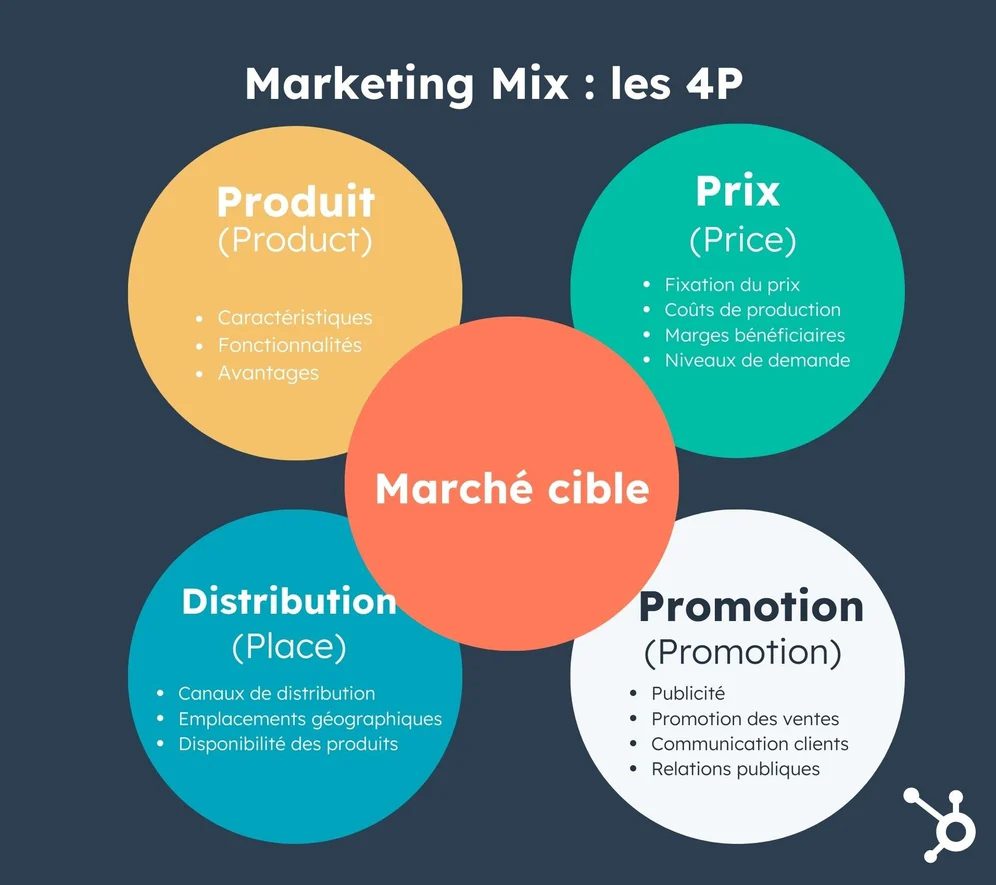
Source : https://blog.hubspot.fr/marketing/marketing-mix
3) Qui bénéficient de ces études ?
Deux grandes familles de pionniers obtiennent le meilleur ROI (retour sur investissement) de ces études : startupers santé (par exemple cliniciens‑, ingénieurs, étudiants, designers, parfois patients entrepreneurs) et chefs produits ou business unit d’entreprises développant des solutions ou dispositifs médicaux. Les mécaniques d’adoption sont différentes mais complémentaires.
3.1 Startuper santé (eg. clinicien, ingénieur, patient, designer, …)
- Besoins : valider un besoin robuste, définir et clarifier sa proposition de valeur, formaliser les critères d’acceptabilité clinique, cadrer le périmètre réglementaire, tester l’usabilité et l’ancrage dans le parcours de soin.
- Pain points : biais « solutionniste » (tendance à focaliser sur le produit plus que sur le besoin), accès limité aux contextes réels, difficultés à documenter des preuves qualitatives crédibles pour partenaires et investisseurs.
- Approche de dérisquage un processus « need‑driven » inspiré de Stanford Biodesign (immersion, entretiens, observation, criblage de besoins, tests itératifs) qui tient compte également des voies réglementaire et remboursement dès le départ. [biodesigng…anford.edu]
3.2 Chef·fe produit / Business Unit (dédiées aux dispositifs médicaux /pharma/digital)
- Besoins : optimiser le positionnement d’un produit/indication, lever les frictions d’usage en milieu hospitalier, affiner le storytelling médical pour KOLs/payeurs, prioriser les fonctionnalités qui déplacent l’adoption.
- Pain points : inerties internes, silos entre les différents départements clés comme les affaires médicales, le marketing, la R&D ; besoin d’insights transverses fiables pour arbitrer rapidement.
- Approche de dérisquage: des focus groups ou des panels d’experts multi‑parties prenantes (HCPs, bioméd, acheteurs, patients, pharmaciens) et des tests de parcours (de découverte, d’achat, utilisateur, onboarding), pour aligner evidence, produit, accès.
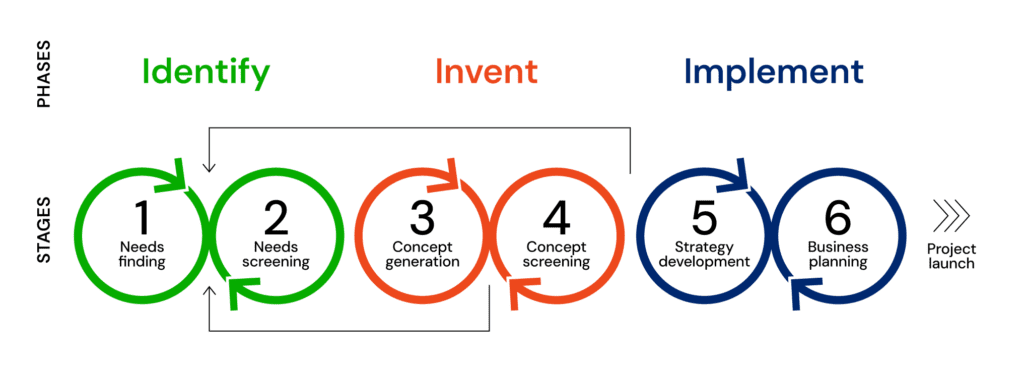
Source : [med.stanford.edu]
4) Une boîte à outils pour répondre à des questions essentielles
La force du qualitatif réside dans la méthode s’appuyant sur les éléments suivants :
Définition du besoin (need statement), des populations (patients/professionnels), scénarii d’usage, hypothèses de valeur et d’acceptabilité.
Nous surfons sur les cadres Human Centered Desgin / Design Thinking validés en milieu clinique et proposons les services suivants choisis de façon propre à chaque projet après analyse des besoins de celui-ci en fonction de son stade de développement.
- Immersions
Shadowing in situ (service hospitalier, consultation, domicile, pharmacie hospitalière.), observation des workflows et points de friction. - Entretiens semi‑directifs professionnels de santé/utilisateurs. Rendre visibles les déterminants d’usage non mesurés par les questionnaires.
- Tests d’usage / facteurs humains )
Développement de Scénarii, mis en exergue des tâches critiques, mesure d’erreurs et de récupérabilité, verbatims, consolidation vers exigences d’interfaces et « Instructions For Use ». - Ateliers de co‑conception
Conceptualisation rapide, itérations guidées par feedbacks. - Panel d’experts et Focus Group
Réunion d’experts ou de professionnels de différents profils autour d’un même sujet, avec codage des thèmes abordés (bénéfices perçus, risques, charge cognitive, compatibilité workflow, déclencheurs d’essai, preuves attendues, incitations économiques), impacts prioritaires sur produit, accès, evidence, ‑go‑tomarket… - Simulation
Recréer l’environnement réel et prendre le temps de l’analyser en dehors de tout risque avec des professionnels, des patients simulés et un environnement hospitalier ou de domicile recréé, comment itérer après les premiers déploiements (sites pilotes). - Préparation à la mise en place d’un pilote. Définition de la fréquence des évaluations et des indicateurs d’implémentation adaptés.
L’ensemble de ces outils finement choisis doit permettre de répondre à toutes les questions nécessaires à un déploiement réussi : depuis la validation du besoin, la validation de la solution dans sa nature et son format, puis définition qui convaincre, avec quelle preuve, par quel canal, à quel moment.
5) Comment H4 opère pour vous
Le Design Thinking n’est pas un « atelier post-‑it ». C’est une discipline de recherche qualitative, prototypage et apprentissage rapide, parfaitement adaptée aux systèmes de soins. Les apports sont prouvés : meilleure compréhension des besoins, réduction des inégalités d’accès, équipes alignées et plus créatives face à la complexité.
Le processus Biodesign (Stanford) en est une référence opérationnelle : identifier (immersion/entretiens), inventer (idéation/prototypage/tests), implémenter (trajets réglementaires/remboursement, modèle d’affaires). Les fellows Biodesign démarrent par des centaines de besoins observés, puis filtrent rigoureusement avant même d’entrer en solution. C’est exactement cette rigueur « need‑driven » que nous appliquons avec nos clients.
Notre positionnement : H4, Hands-On Human Health Hub permet de connecter les entrepreneurs, au sens large, avec les professionnels oeuvrant dans le milieu de la santé. Le Hands-On correspond à ces études de marché qualitatives au service des startupers santé et des entreprises (medtech, e‑santé, pharma, diagnostics). Nous ne sommes pas un incubateur/accélérateur ; nous travaillons avec eux et avec vos équipes pour documenter l’adoption et accélérer la validation.
Les bénéfices observés sont notamment :
- Biais solutionniste bridé : vous investissez sur des besoins validés.
- Décisions plus rapides : arbitrages produit/accès guidés par insights « riches ».
- Adoption renforcée : message, workflow, formation, evidence alignés avec les réalités terrains.
6) FAQ
« Le qualitatif, c’est subjectif »
Les méthodes qualitatives suivent des protocoles éprouvés (guides d’entretien, saturation théorique, double codage, triangulation) publiés dans des revues dédiées (Qualitative Health Research) et encouragées par les journaux cliniques. Leur rigueur tient à la transparence des étapes et à la traçabilité des données.
« On préfère un N=500 »
Les questionnaires quanti sont précieux… quand on sait quoi mesurer. Le quali intervient en amont pour formuler les bonnes questions (langage, attributs, scénarios), réduire le bruit et éviter les biais de formulation.
« On connaît notre marché »
L’adoption dépend de signaux faibles (usages réels, micro‑contraintes de service, incitations) souvent invisibles depuis le bureau. Le terrain révèle rapidement ce qui bloque ou débloque. Des éditoriaux récents pointent que sans ce travail, même des innovations pertinentes peinent à diffuser.
7) Checklist : Êtes‑vous prêt à dérisquer votre innovation santé ?
- Need statement clair, validé auprès de ≥ 3 catégories d’utilisateurs (patients, HCPs, acheteurs) ?
- Scénarios d’usage mappés (lieux, acteurs, tâches critiques, risques) ?
- Preuves attendues par payeurs/Méthodes d’évaluation identifiées (outcomes, ressources consommées, organisation) ?
- Drivers & freins d’adoption documentés (confiance, valeur perçue, interopérabilité, formation) ?
- KOLs & ambassadeurs cartographiés, messages testés ?
- Plan d’évaluation des premiers déploiements (indicateurs d’implémentation, retours d’expérience) ?
Si vous avez des « non » : commencez par une phase qualitative. Deux à quatre semaines suffisent souvent pour réduire la zone d’incertitude et orienter efficacement la suite (quanti, études cliniques, business case).
En conclusion : la voie la plus rapide vers l’adoption… c’est de prendre le temps au début
L’innovation santé échoue rarement par manque de technologie ; elle échoue parce qu’elle n’épouse pas assez tôt les réalités humaines, cliniques et économiques du soin. Les études de marché qualitatives constituent la phase zéro du risque : elles évitent les paris mal informés, révèlent les leviers d’adoption et font gagner des mois sur la route de l’accès au marché.
Références (sélection)
-
Valeur de la recherche qualitative en contexte clinique et épidémiologique : Clinical Kidney Journal (2025) ; The Lancet Regional Health (2023). [academic.oup.com], [thelancet.com]
-
Design Thinking / HCD en santé : BMJ Innovations (revue systématique) ; Journal of General Internal Medicine (2024). [innovations.bmj.com], [link.springer.com]
-
Adoption digitale en santé et barrières : Frontiers in Digital Health (2024) ; Translational Behavioral Medicine (2025) ; EJBI (2024). [frontiersin.org], [academic.oup.com], [ejbi.org]
-
Processus Biodesign (need‑driven) : Stanford Medicine ; Guide Biodesign ; conf. Stanford Biodesign. [med.stanford.edu], [biodesigng…anford.edu]
-
Usability / facteurs humains pour DM : IEC 62366‑1 (ISO/IEC) ; Greenlight Guru (synthèse). [iso.org], [greenlight.guru]
-
Accès au marché & lancements : Deloitte Insights (MA & launch) ; Medical Affairs (rôle stratégique). [deloitte.com], [linkedin.com]
